โรคแค็กเซีย (Cachexia) เป็นโรคทางระบบที่มีอาการหลัก คือ น้ำหนักลด กล้ามเนื้อและเนื้อเยื่อไขมันฝ่อตัวลง และการอักเสบของระบบ โรคแค็กเซียเป็นหนึ่งในภาวะแทรกซ้อนและสาเหตุการเสียชีวิตหลักในผู้ป่วยมะเร็ง คาดการณ์ว่าอุบัติการณ์ของภาวะแค็กเซียในผู้ป่วยมะเร็งอาจสูงถึง 25% ถึง 70% และในแต่ละปีมีผู้ป่วยโรคแค็กเซียทั่วโลกประมาณ 9 ล้านคน โดย 80% คาดว่าจะเสียชีวิตภายในหนึ่งปีหลังการวินิจฉัย นอกจากนี้ โรคแค็กเซียยังส่งผลกระทบอย่างมีนัยสำคัญต่อคุณภาพชีวิตของผู้ป่วย (QOL) และทำให้ภาวะพิษจากการรักษารุนแรงขึ้น
การแทรกแซงภาวะแค็กเซียอย่างมีประสิทธิภาพมีความสำคัญอย่างยิ่งต่อการพัฒนาคุณภาพชีวิตและการพยากรณ์โรคของผู้ป่วยโรคมะเร็ง อย่างไรก็ตาม แม้จะมีความก้าวหน้าในการศึกษากลไกทางพยาธิสรีรวิทยาของภาวะแค็กเซีย แต่ยาหลายชนิดที่พัฒนาขึ้นโดยอาศัยกลไกที่เป็นไปได้กลับมีประสิทธิภาพเพียงบางส่วนหรือไม่ได้ประสิทธิภาพ ปัจจุบันยังไม่มีวิธีการรักษาที่มีประสิทธิภาพที่ได้รับการรับรองจากสำนักงานคณะกรรมการอาหารและยาแห่งสหรัฐอเมริกา (FDA)
ภาวะผอมแห้ง (Cachexia) มักพบได้บ่อยในผู้ป่วยมะเร็งหลายชนิด ซึ่งมักส่งผลให้น้ำหนักลด กล้ามเนื้อลีบ คุณภาพชีวิตลดลง สมรรถภาพการทำงานลดลง และอัตราการรอดชีวิตลดลง ตามมาตรฐานสากลที่ยอมรับกัน ภาวะนี้ถูกกำหนดให้มีค่าดัชนีมวลกาย (BMI, น้ำหนัก [กก.] หารด้วยส่วนสูง [ม.] ยกกำลังสอง) น้อยกว่า 20 หรือในผู้ป่วยภาวะซาร์โคพีเนีย คือ น้ำหนักลดลงมากกว่า 5% ภายในหกเดือน หรือน้ำหนักลดลงมากกว่า 2% ปัจจุบันยังไม่มียาใดได้รับการอนุมัติในสหรัฐอเมริกาและยุโรปสำหรับรักษาภาวะผอมแห้งจากมะเร็งโดยเฉพาะ ทำให้มีทางเลือกในการรักษาที่จำกัด
แนวทางล่าสุดที่แนะนำให้ใช้โอแลนซาปีนขนาดต่ำเพื่อเพิ่มความอยากอาหารและน้ำหนักในผู้ป่วยมะเร็งระยะลุกลาม ส่วนใหญ่อ้างอิงจากผลการศึกษาแบบศูนย์เดียว นอกจากนี้ การใช้อะนาล็อกของโปรเจสเตอโรนหรือกลูโคคอร์ติคอยด์ในระยะสั้นอาจให้ประโยชน์ได้จำกัด แต่ก็มีความเสี่ยงที่จะเกิดผลข้างเคียงที่ไม่พึงประสงค์ (เช่น การใช้โปรเจสเตอโรนที่เกี่ยวข้องกับภาวะลิ่มเลือดอุดตัน) การทดลองทางคลินิกของยาอื่นๆ ยังไม่แสดงให้เห็นถึงประสิทธิภาพเพียงพอที่จะได้รับการอนุมัติจากหน่วยงานกำกับดูแล แม้ว่าอะนามอรีน (อะนามอรีน) (เปปไทด์ที่ปลดปล่อยฮอร์โมนการเจริญเติบโตในรูปแบบรับประทาน) จะได้รับการอนุมัติในญี่ปุ่นสำหรับการรักษาภาวะแค็กเซียจากมะเร็ง แต่ยานี้เพียงแค่เพิ่มองค์ประกอบของร่างกายในระดับหนึ่ง ไม่ได้เพิ่มความแข็งแรงของมือ และท้ายที่สุดก็ไม่ได้รับการอนุมัติจากสำนักงานคณะกรรมการอาหารและยาแห่งสหรัฐอเมริกา (FDA) ดังนั้นจึงมีความจำเป็นเร่งด่วนในการรักษาภาวะแค็กเซียจากมะเร็งที่ปลอดภัย มีประสิทธิภาพ และตรงจุด
ปัจจัยการเจริญเติบโตที่ทำให้เกิดความแตกต่าง 15 (GDF-15) เป็นไซโตไคน์ที่เกิดจากความเครียด ซึ่งจับกับโปรตีนที่คล้ายตัวรับในกลุ่มปัจจัยการเจริญเติบโตของเส้นประสาท (GFRAL) ที่ได้จากเซลล์เกลียในสมองส่วนหลัง วิถี GDF-15-GFRAL ได้รับการระบุว่าเป็นตัวควบคุมหลักของอาการเบื่ออาหารและการควบคุมน้ำหนัก และมีบทบาทในการเกิดโรคแค็กเซีย ในสัตว์ทดลอง GDF-15 สามารถกระตุ้นให้เกิดโรคแค็กเซียได้ และการยับยั้ง GDF-15 สามารถบรรเทาอาการนี้ได้ นอกจากนี้ ระดับ GDF-15 ที่สูงขึ้นในผู้ป่วยมะเร็งยังสัมพันธ์กับน้ำหนักตัวและมวลกล้ามเนื้อโครงร่างที่ลดลง ความแข็งแรงที่ลดลง และอัตราการรอดชีวิตที่สั้นลง ซึ่งเน้นย้ำถึงคุณค่าของ GDF-15 ในฐานะเป้าหมายการรักษาที่มีศักยภาพ
พอนเซโกรแมบ (PF-06946860) เป็นแอนติบอดีโมโนโคลนอลของมนุษย์ที่มีความจำเพาะสูง สามารถจับกับ GDF-15 ในกระแสเลือด จึงยับยั้งปฏิกิริยากับตัวรับ GFRAL ในการทดลองแบบเปิดขนาดเล็กระยะ 1b ผู้ป่วย 10 รายที่มีภาวะแค็กเซียในมะเร็งและมีระดับ GDF-15 ในกระแสเลือดสูงขึ้น ได้รับการรักษาด้วยพอนเซโกรแมบ และพบว่าน้ำหนักตัว ความอยากอาหาร และการออกกำลังกายดีขึ้น ในขณะที่ระดับ GDF-15 ในซีรัมถูกยับยั้งและอาการไม่พึงประสงค์อยู่ในระดับต่ำ จากข้อมูลนี้ เราจึงได้ทำการทดลองทางคลินิกระยะ 2 เพื่อประเมินความปลอดภัยและประสิทธิภาพของพอนเซโกรแมบในผู้ป่วยภาวะแค็กเซียในมะเร็งที่มีระดับ GDF-15 ในกระแสเลือดสูงขึ้น เมื่อเทียบกับยาหลอก เพื่อทดสอบสมมติฐานที่ว่า GDF-15 เป็นสาเหตุของโรคหลัก
การศึกษานี้รวมถึงผู้ป่วยผู้ใหญ่ที่เป็นโรคแค็กเซียที่เกี่ยวข้องกับมะเร็ง (มะเร็งปอดชนิดไม่ใช่เซลล์เล็ก มะเร็งตับอ่อน หรือมะเร็งลำไส้ใหญ่) ที่มีระดับ GDF-15 ในซีรั่มอย่างน้อย 1,500 pg/ml คะแนนสถานะสมรรถภาพของ Eastern Tumor Consortium (ECOG) ≤3 และมีอายุขัยอย่างน้อย 4 เดือน
ผู้ป่วยที่ลงทะเบียนได้รับการสุ่มให้รับ ponsegromab 3 โดส ขนาด 100 มก., 200 มก. หรือ 400 มก. หรือยาหลอก ฉีดใต้ผิวหนังทุก 4 สัปดาห์ ในอัตราส่วน 1:1:1 จุดยุติหลักคือการเปลี่ยนแปลงของน้ำหนักตัวเทียบกับค่าพื้นฐานที่ 12 สัปดาห์ จุดยุติรองที่สำคัญคือการเปลี่ยนแปลงจากค่าพื้นฐานในคะแนน anorexia cachexia Sub-Scale (FAACT-ACS) ซึ่งเป็นการประเมินการทำงานของการรักษาสำหรับ anorexia cachexia จุดยุติรองอื่นๆ ได้แก่ คะแนนบันทึกอาการของภาวะแค็กเซียที่เกี่ยวข้องกับมะเร็ง การเปลี่ยนแปลงของกิจกรรมทางกายที่เริ่มต้น และจุดยุติการเดิน ซึ่งวัดโดยใช้อุปกรณ์สุขภาพดิจิทัลแบบสวมใส่ได้ ข้อกำหนดระยะเวลาการสวมใส่ขั้นต่ำได้ระบุไว้ล่วงหน้า การประเมินความปลอดภัยประกอบด้วยจำนวนเหตุการณ์ไม่พึงประสงค์ระหว่างการรักษา ผลการตรวจทางห้องปฏิบัติการ สัญญาณชีพ และคลื่นไฟฟ้าหัวใจ จุดสิ้นสุดการสำรวจได้แก่การเปลี่ยนแปลงพื้นฐานของดัชนีของกล้ามเนื้อโครงร่างส่วนเอว (พื้นที่ของกล้ามเนื้อโครงร่างหารด้วยความสูงยกกำลังสอง) ที่เกี่ยวข้องกับกล้ามเนื้อโครงร่างระบบ
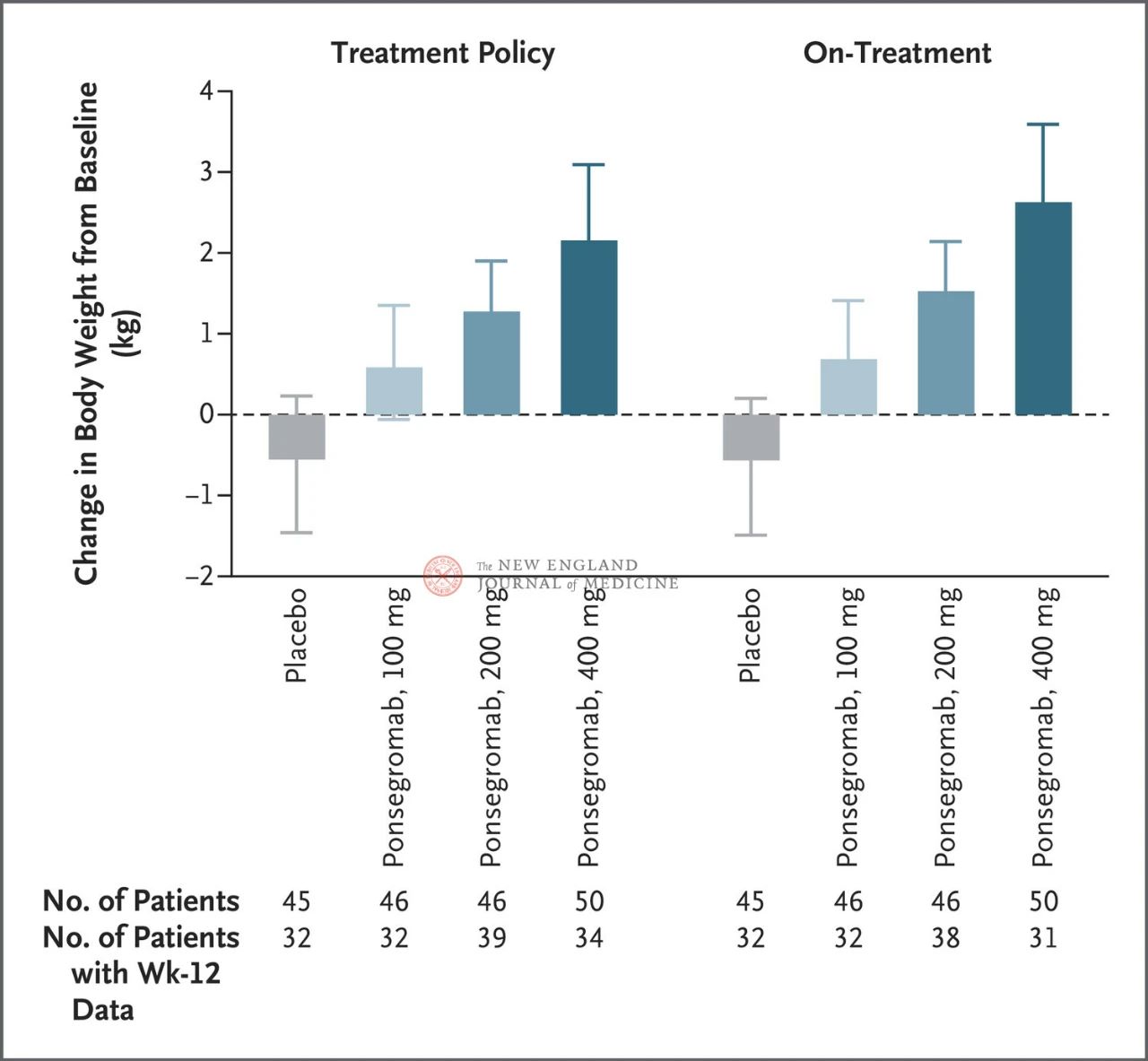
ผู้ป่วยทั้งหมด 187 รายได้รับการสุ่มให้รับพอนเซโกรแมบ 100 มก. (46 ราย), 200 มก. (46 ราย), 400 มก. (50 ราย) หรือยาหลอก (45 ราย) ผู้ป่วย 74 ราย (ร้อยละ 40) เป็นมะเร็งปอดชนิดไม่ใช่เซลล์เล็ก 59 ราย (ร้อยละ 32) เป็นมะเร็งตับอ่อน และ 54 ราย (ร้อยละ 29) เป็นมะเร็งลำไส้ใหญ่และทวารหนัก
ความแตกต่างระหว่างกลุ่ม 100 มก., 200 มก. และ 400 มก. กับกลุ่มยาหลอกคือ 1.22 กก., 1.92 กก. และ 2.81 กก. ตามลำดับ
ภาพแสดงจุดสิ้นสุดปฐมภูมิ (การเปลี่ยนแปลงของน้ำหนักตัวจากช่วงเริ่มต้นถึง 12 สัปดาห์) สำหรับผู้ป่วยมะเร็งแค็กเซียในกลุ่มที่ได้รับพอนเซโกรแมบและกลุ่มยาหลอก หลังจากปรับค่าความเสี่ยงต่อการเสียชีวิตและเหตุการณ์อื่นๆ ที่เกิดขึ้นพร้อมกัน เช่น การหยุดการรักษา จุดสิ้นสุดปฐมภูมิได้รับการวิเคราะห์โดยใช้แบบจำลอง Emax แบบแบ่งกลุ่ม (stratified Emax model) โดยใช้ผลการวิเคราะห์ตามยาวแบบ Bayesian joint ในสัปดาห์ที่ 12 (ซ้าย) จุดสิ้นสุดปฐมภูมิได้รับการวิเคราะห์ในลักษณะเดียวกัน โดยใช้เป้าหมายที่ประมาณการไว้สำหรับการรักษาจริง โดยตัดทอนค่าการสังเกตหลังจากเหตุการณ์ที่เกิดขึ้นพร้อมกันทั้งหมด (ภาพขวา) ช่วงความเชื่อมั่น (ระบุไว้ในบทความ)
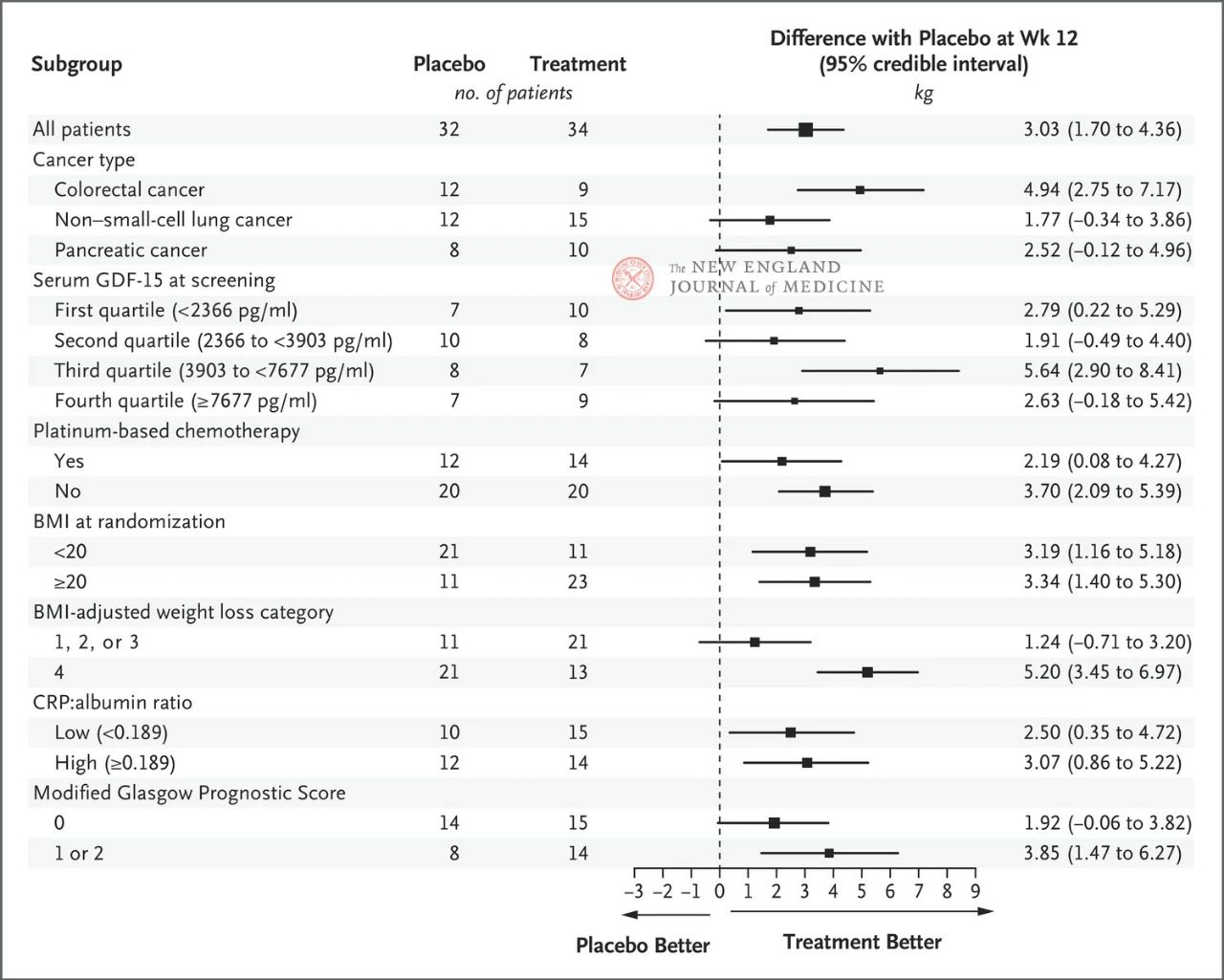
ผลของพอนเซโกรแมบขนาด 400 มิลลิกรัมต่อน้ำหนักตัวมีความสอดคล้องกันในกลุ่มย่อยหลักที่กำหนดไว้ล่วงหน้า ได้แก่ ชนิดของมะเร็ง ระดับ GDF-15 ในซีรัม ระดับการได้รับเคมีบำบัดแบบแพลตตินัม ดัชนีมวลกาย และการอักเสบของระบบพื้นฐาน การเปลี่ยนแปลงของน้ำหนักสอดคล้องกับการยับยั้ง GDF-15 ที่ 12 สัปดาห์
การคัดเลือกกลุ่มย่อยหลักๆ อิงตามการวิเคราะห์แบบเบย์เซียนร่วมตามยาวแบบโพสต์ฮอค ซึ่งดำเนินการหลังจากปรับค่าความเสี่ยงการเสียชีวิตจากการแข่งขันตามเป้าหมายที่ประมาณการไว้ของกลยุทธ์การรักษาแล้ว ไม่ควรใช้ช่วงความเชื่อมั่นแทนการทดสอบสมมติฐานที่ไม่มีการปรับค่าหลายครั้ง ดัชนีมวลกาย (BMI) แทนดัชนีมวลกาย CRP แทนโปรตีนซี-รีแอคทีฟ และ GDF-15 แทนปัจจัยการเจริญเติบโตที่แตกต่าง 15
ในช่วงเริ่มต้น ผู้ป่วยในกลุ่มที่ได้รับพอนเซโกรแมบขนาด 200 มิลลิกรัมมีสัดส่วนที่สูงกว่าที่รายงานว่าความอยากอาหารไม่ลดลง เมื่อเทียบกับกลุ่มที่ได้รับยาหลอก ผู้ป่วยในกลุ่มที่ได้รับพอนเซโกรแมบขนาด 100 มิลลิกรัมและ 400 มิลลิกรัมรายงานว่าความอยากอาหารดีขึ้นจากช่วงเริ่มต้นที่ 12 สัปดาห์ โดยมีคะแนน FAACT-ACS เพิ่มขึ้น 4.12 และ 4.5077 ตามลำดับ ไม่พบความแตกต่างอย่างมีนัยสำคัญในคะแนน FAACT-ACS ระหว่างกลุ่มที่ได้รับยา 200 มิลลิกรัมและกลุ่มที่ได้รับยาหลอก
เนื่องจากข้อกำหนดระยะเวลาการสวมใส่ที่กำหนดไว้ล่วงหน้าและปัญหาเกี่ยวกับอุปกรณ์ ผู้ป่วย 59 และ 68 รายตามลำดับจึงได้ให้ข้อมูลเกี่ยวกับการเปลี่ยนแปลงของกิจกรรมทางกายและจุดสิ้นสุดของการเดินเมื่อเทียบกับค่าพื้นฐาน ในกลุ่มผู้ป่วยเหล่านี้ เมื่อเปรียบเทียบกับกลุ่มที่ได้รับยาหลอก ผู้ป่วยในกลุ่มที่ได้รับยา 400 มิลลิกรัมมีกิจกรรมโดยรวมเพิ่มขึ้นที่ 12 สัปดาห์ โดยมีกิจกรรมทางกายที่ไม่ได้เคลื่อนไหวเพิ่มขึ้น 72 นาทีต่อวัน นอกจากนี้ กลุ่มที่ได้รับยา 400 มิลลิกรัมยังมีดัชนีกล้ามเนื้อโครงร่างส่วนเอวเพิ่มขึ้นที่ 12 สัปดาห์อีกด้วย
อุบัติการณ์ของอาการไม่พึงประสงค์อยู่ที่ 70% ในกลุ่มที่ได้รับพอนเซโกรแมบ เทียบกับ 80% ในกลุ่มที่ได้รับยาหลอก และเกิดขึ้นในผู้ป่วย 90% ที่ได้รับยาต้านมะเร็งแบบระบบพร้อมกัน อุบัติการณ์ของอาการคลื่นไส้และอาเจียนต่ำกว่าในกลุ่มที่ได้รับพอนเซโกรแมบ
เวลาโพสต์: 05 ต.ค. 2567