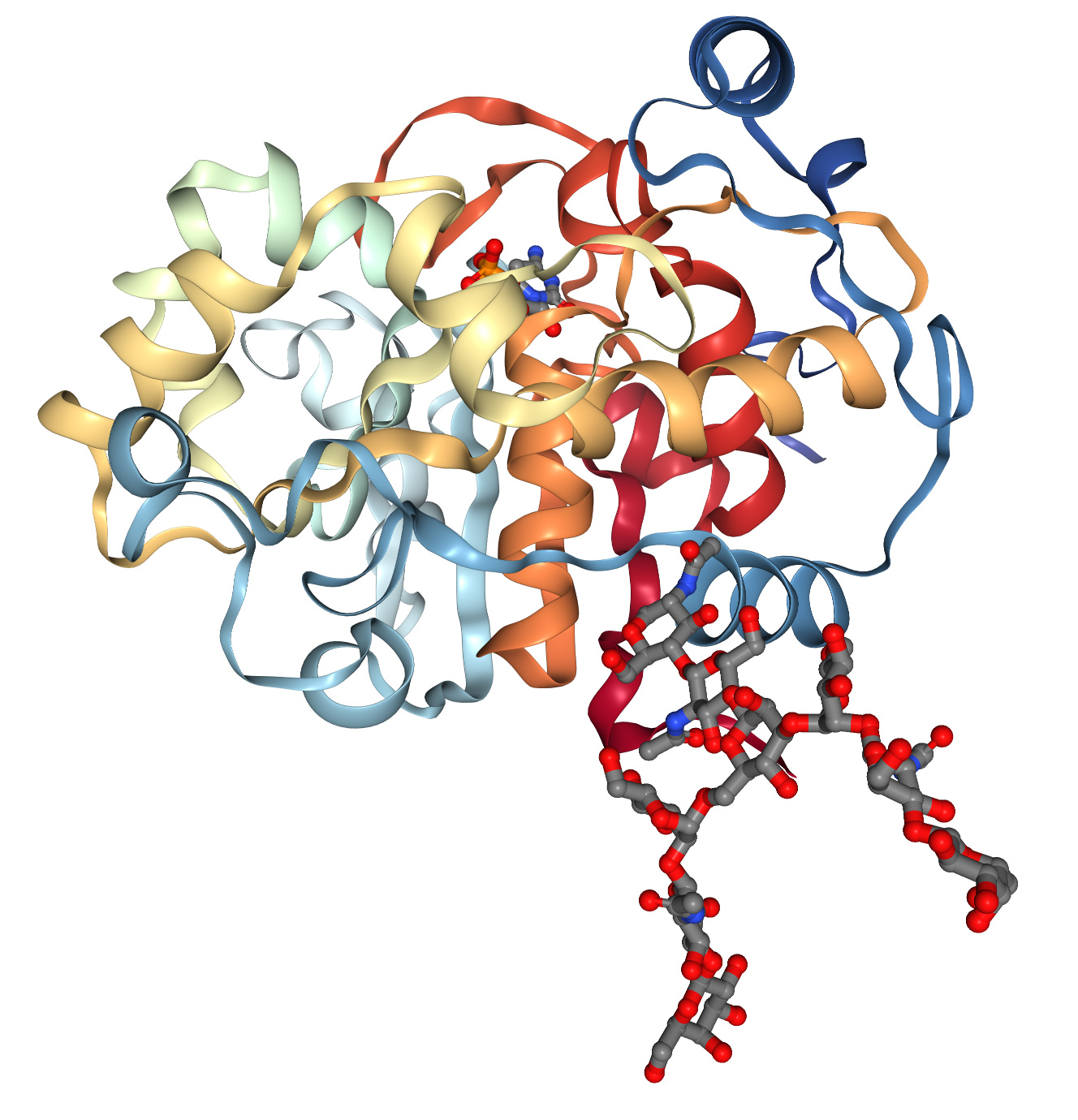
รางวัล Lasker Basic Medical Research Award ของปีนี้มอบให้แก่ Demis Hassabis และ John Jumper สำหรับผลงานในการสร้างระบบปัญญาประดิษฐ์ AlphaFold ที่สามารถทำนายโครงสร้างสามมิติของโปรตีนโดยอ้างอิงจากลำดับกรดอะมิโนอันดับแรก
ผลการวิจัยของพวกเขาช่วยแก้ปัญหาที่รบกวนวงการวิทยาศาสตร์มานาน และเปิดประตูสู่การเร่งรัดการวิจัยในสาขาชีวการแพทย์ โปรตีนมีบทบาทสำคัญในการพัฒนาของโรค ในโรคอัลไซเมอร์ โปรตีนจะพับตัวและเกาะกลุ่มกัน ในโรคมะเร็ง หน้าที่ควบคุมของโปรตีนจะสูญหายไป ในโรคเมตาบอลิซึมแต่กำเนิด โปรตีนจะทำงานผิดปกติ ในโรคซิสติกไฟโบรซิส โปรตีนจะเข้าไปอยู่ในช่องว่างที่ไม่ถูกต้องในเซลล์ นี่เป็นเพียงส่วนหนึ่งของกลไกมากมายที่ก่อให้เกิดโรค แบบจำลองโครงสร้างโปรตีนโดยละเอียดสามารถให้โครงสร้างอะตอม ขับเคลื่อนการออกแบบหรือการคัดเลือกโมเลกุลที่มีความสัมพันธ์สูง และเร่งการค้นพบยา
โดยทั่วไปโครงสร้างโปรตีนจะถูกกำหนดโดยเทคนิคผลึกศาสตร์รังสีเอกซ์ เรโซแนนซ์แม่เหล็กนิวเคลียร์ และกล้องจุลทรรศน์อิเล็กตรอนแบบแช่แข็ง วิธีการเหล่านี้มีราคาแพงและใช้เวลานาน ส่งผลให้ฐานข้อมูลโครงสร้างโปรตีนสามมิติที่มีอยู่มีข้อมูลโครงสร้างเพียงประมาณ 200,000 รายการ ในขณะที่เทคโนโลยีการจัดลำดับดีเอ็นเอสามารถผลิตลำดับโปรตีนได้มากกว่า 8 ล้านลำดับ ในช่วงทศวรรษ 1960 Anfinsen และคณะได้ค้นพบว่าลำดับกรดอะมิโน 1 มิติสามารถพับตัวได้เองและซ้ำๆ กันเป็นโครงสร้างสามมิติที่ใช้งานได้ (รูปที่ 1A) และ “แชเปอโรน” ในระดับโมเลกุลสามารถเร่งและอำนวยความสะดวกให้กับกระบวนการนี้ได้ ข้อสังเกตเหล่านี้นำไปสู่ความท้าทายทางชีววิทยาโมเลกุลที่ดำเนินมายาวนานถึง 60 ปี นั่นคือการทำนายโครงสร้างสามมิติของโปรตีนจากลำดับกรดอะมิโน 1 มิติ ด้วยความสำเร็จของโครงการจีโนมมนุษย์ ความสามารถของเราในการได้มาซึ่งลำดับกรดอะมิโน 1 มิติจึงได้รับการพัฒนาขึ้นอย่างมาก และความท้าทายนี้ก็ยิ่งเร่งด่วนมากขึ้นไปอีก
การทำนายโครงสร้างของโปรตีนเป็นเรื่องยากด้วยเหตุผลหลายประการ ประการแรก ตำแหน่งสามมิติที่เป็นไปได้ทั้งหมดของอะตอมในกรดอะมิโนแต่ละชนิดจำเป็นต้องอาศัยการศึกษาค้นคว้าอย่างมาก ประการที่สอง โปรตีนใช้ประโยชน์จากองค์ประกอบเชิงเติมเต็มในโครงสร้างทางเคมีอย่างเต็มที่เพื่อจัดโครงสร้างอะตอมอย่างมีประสิทธิภาพ เนื่องจากโปรตีนโดยทั่วไปมี “ผู้ให้” พันธะไฮโดรเจนหลายร้อยตัว (โดยปกติคือออกซิเจน) ซึ่งควรจะอยู่ใกล้กับ “ตัวรับ” พันธะไฮโดรเจน (โดยปกติคือไนโตรเจนที่ยึดกับไฮโดรเจน) จึงอาจเป็นเรื่องยากมากที่จะหาโครงสร้างที่ผู้ให้เกือบทั้งหมดอยู่ใกล้กับตัวรับ ประการที่สาม มีตัวอย่างจำกัดสำหรับการฝึกอบรมวิธีการทดลอง ดังนั้นจึงจำเป็นต้องเข้าใจปฏิสัมพันธ์สามมิติที่อาจเกิดขึ้นระหว่างกรดอะมิโนโดยอาศัยลำดับ 1 มิติ โดยใช้ข้อมูลเกี่ยวกับวิวัฒนาการของโปรตีนที่เกี่ยวข้อง
ฟิสิกส์ถูกนำมาใช้เป็นแบบจำลองปฏิกิริยาระหว่างอะตอมในการค้นหาโครงสร้างที่ดีที่สุดเป็นครั้งแรก และได้มีการพัฒนาวิธีการทำนายโครงสร้างของโปรตีนขึ้นมา Karplus, Levitt และ Warshel ได้รับรางวัลโนเบลสาขาเคมีประจำปี 2013 จากผลงานการจำลองโปรตีนด้วยคอมพิวเตอร์ อย่างไรก็ตาม วิธีการที่ใช้ฟิสิกส์มีค่าใช้จ่ายสูงและต้องใช้การประมวลผลโดยประมาณ ดังนั้นจึงไม่สามารถทำนายโครงสร้างสามมิติที่แม่นยำได้ อีกวิธีหนึ่งที่ “อิงความรู้” คือการใช้ฐานข้อมูลโครงสร้างและลำดับที่รู้จัก เพื่อฝึกฝนแบบจำลองผ่านปัญญาประดิษฐ์และการเรียนรู้ของเครื่อง (AI-ML) Hassabis และ Jumper ได้นำองค์ประกอบทั้งทางฟิสิกส์และ AI-ML มาใช้ แต่นวัตกรรมและประสิทธิภาพที่ก้าวกระโดดของวิธีการนี้ส่วนใหญ่มาจาก AI-ML นักวิจัยทั้งสองได้ผสมผสานฐานข้อมูลสาธารณะขนาดใหญ่เข้ากับทรัพยากรคอมพิวเตอร์ระดับอุตสาหกรรมอย่างสร้างสรรค์เพื่อสร้าง AlphaFold
เราจะรู้ได้อย่างไรว่าพวกเขาได้ "ไข" ปริศนาการทำนายโครงสร้างแล้ว? ในปี 1994 การแข่งขัน Critical Assessment of Structure Prediction (CASP) ได้ถูกจัดตั้งขึ้น ซึ่งจัดขึ้นทุกสองปีเพื่อติดตามความคืบหน้าของการทำนายโครงสร้าง นักวิจัยจะแบ่งปันลำดับเบส 1 มิติของโปรตีนที่พวกเขาเพิ่งค้นพบโครงสร้าง แต่ผลการวิจัยยังไม่ได้รับการเผยแพร่ ผู้ทำนายจะทำนายโครงสร้างสามมิติโดยใช้ลำดับเบส 1 มิตินี้ และผู้ประเมินจะประเมินคุณภาพของผลลัพธ์ที่ทำนายโดยอิสระโดยการเปรียบเทียบกับโครงสร้างสามมิติที่ผู้ทดลองให้ไว้ (ซึ่งมอบให้เฉพาะผู้ประเมินเท่านั้น) CASP ดำเนินการตรวจสอบแบบปิดบังข้อมูลอย่างแท้จริงและบันทึกความก้าวหน้าของประสิทธิภาพเป็นระยะๆ ที่เกี่ยวข้องกับนวัตกรรมเชิงวิธีการ ในการประชุม CASP ครั้งที่ 14 ในปี 2020 ผลการทำนายของ AlphaFold แสดงให้เห็นถึงประสิทธิภาพที่ก้าวกระโดดอย่างมาก จนผู้จัดงานประกาศว่าปัญหาการทำนายโครงสร้างสามมิติได้รับการแก้ไขแล้ว ความแม่นยำของการทำนายส่วนใหญ่ใกล้เคียงกับการวัดในการทดลอง
ความสำคัญที่กว้างกว่านั้นคือ ผลงานของ Hassabis และ Jumper แสดงให้เห็นอย่างชัดเจนว่า AI-ML สามารถเปลี่ยนแปลงวิทยาศาสตร์ได้อย่างไร งานวิจัยแสดงให้เห็นว่า AI-ML สามารถสร้างสมมติฐานทางวิทยาศาสตร์ที่ซับซ้อนจากแหล่งข้อมูลหลายแหล่ง กลไกการใส่ใจ (เช่นเดียวกับใน ChatGPT) สามารถค้นพบความสัมพันธ์และความสัมพันธ์ที่สำคัญในแหล่งข้อมูล และ AI-ML สามารถตัดสินคุณภาพของผลลัพธ์ได้ด้วยตนเอง AI-ML คือการทำงานทางวิทยาศาสตร์อย่างแท้จริง
เวลาโพสต์: 23 ก.ย. 2566