การปลูกถ่ายปอดเป็นวิธีการรักษาโรคปอดระยะลุกลามที่ได้รับการยอมรับ ในช่วงไม่กี่ทศวรรษที่ผ่านมา การปลูกถ่ายปอดมีความก้าวหน้าอย่างมากในด้านการคัดกรองและประเมินผู้รับการปลูกถ่าย การคัดเลือก การเก็บรักษา และการจัดสรรปอดของผู้บริจาค เทคนิคการผ่าตัด การจัดการหลังการผ่าตัด การจัดการภาวะแทรกซ้อน และภาวะภูมิคุ้มกันบกพร่อง
กว่า 60 ปี การปลูกถ่ายปอดได้พัฒนาจากการรักษาแบบทดลองไปสู่การรักษามาตรฐานที่ได้รับการยอมรับสำหรับโรคปอดที่คุกคามชีวิต แม้จะมีปัญหาที่พบบ่อย เช่น ภาวะบกพร่องของการปลูกถ่ายอวัยวะหลัก ภาวะบกพร่องของปอดจากการปลูกถ่ายเรื้อรัง (CLAD) ความเสี่ยงที่เพิ่มขึ้นของการติดเชื้อฉวยโอกาส มะเร็ง และปัญหาสุขภาพเรื้อรังที่เกี่ยวข้องกับภาวะภูมิคุ้มกันบกพร่อง แต่ก็มีแนวโน้มที่จะช่วยปรับปรุงอัตราการรอดชีวิตและคุณภาพชีวิตของผู้ป่วยผ่านการคัดเลือกผู้รับที่เหมาะสม แม้ว่าการปลูกถ่ายปอดจะแพร่หลายมากขึ้นทั่วโลก แต่จำนวนการผ่าตัดยังคงไม่สอดคล้องกับความต้องการที่เพิ่มขึ้น บทความนี้มุ่งเน้นไปที่สถานะปัจจุบันและความก้าวหน้าล่าสุดในการปลูกถ่ายปอด รวมถึงโอกาสในอนาคตสำหรับการนำวิธีการรักษาที่ท้าทายแต่อาจเปลี่ยนแปลงชีวิตนี้ไปใช้อย่างมีประสิทธิภาพ
การประเมินและการคัดเลือกผู้รับที่มีศักยภาพ
เนื่องจากปอดของผู้บริจาคที่เหมาะสมนั้นค่อนข้างหายาก ศูนย์ปลูกถ่ายอวัยวะจึงมีหน้าที่ทางจริยธรรมในการจัดสรรอวัยวะของผู้บริจาคให้แก่ผู้รับที่มีศักยภาพซึ่งมีแนวโน้มที่จะได้รับประโยชน์สุทธิจากการปลูกถ่ายมากที่สุด นิยามดั้งเดิมของผู้รับที่มีศักยภาพเหล่านี้คือมีความเสี่ยงโดยประมาณมากกว่า 50% ที่จะเสียชีวิตจากโรคปอดภายใน 2 ปี และมีโอกาสมากกว่า 80% ที่จะมีชีวิตรอดหลังจากการปลูกถ่าย 5 ปี โดยสมมติว่าปอดที่ปลูกถ่ายสามารถทำงานได้อย่างสมบูรณ์ ข้อบ่งชี้ที่พบบ่อยที่สุดสำหรับการปลูกถ่ายปอด ได้แก่ โรคพังผืดในปอด โรคปอดอุดกั้นเรื้อรัง โรคหลอดเลือดในปอด และโรคซิสติกไฟโบรซิส ผู้ป่วยจะได้รับการส่งต่อโดยพิจารณาจากการทำงานของปอดที่ลดลง การทำงานของร่างกายที่ลดลง และความก้าวหน้าของโรค แม้จะใช้ยาและการผ่าตัดมากที่สุดก็ตาม นอกจากนี้ยังมีการพิจารณาเกณฑ์เฉพาะโรคอื่นๆ ความท้าทายในการพยากรณ์โรคสนับสนุนกลยุทธ์การส่งต่อตั้งแต่เนิ่นๆ ซึ่งช่วยให้สามารถให้คำปรึกษาด้านความเสี่ยงและผลประโยชน์ที่ดีขึ้น เพื่อปรับปรุงการตัดสินใจร่วมกันอย่างมีข้อมูล และโอกาสในการเปลี่ยนแปลงอุปสรรคที่อาจเกิดขึ้นต่อผลลัพธ์ของการปลูกถ่ายที่ประสบความสำเร็จ ทีมสหสาขาวิชาชีพจะประเมินความจำเป็นในการปลูกถ่ายปอดและความเสี่ยงของผู้ป่วยต่อภาวะแทรกซ้อนหลังการปลูกถ่ายอันเนื่องมาจากการใช้ยากดภูมิคุ้มกัน เช่น ความเสี่ยงต่อการติดเชื้อที่อาจเป็นอันตรายถึงชีวิต การคัดกรองภาวะผิดปกติของอวัยวะภายนอกปอด สมรรถภาพทางกาย สุขภาพจิต ภูมิคุ้มกันของร่างกาย และมะเร็งเป็นสิ่งสำคัญยิ่ง การประเมินเฉพาะด้านของหลอดเลือดหัวใจและหลอดเลือดสมอง การทำงานของไต สุขภาพกระดูก การทำงานของหลอดอาหาร สมรรถภาพทางจิตสังคม และการสนับสนุนทางสังคมเป็นสิ่งสำคัญยิ่ง ในขณะเดียวกันก็ให้ความสำคัญกับความโปร่งใส เพื่อหลีกเลี่ยงความไม่เท่าเทียมในการพิจารณาความเหมาะสมสำหรับการปลูกถ่าย
ปัจจัยเสี่ยงหลายประการเป็นอันตรายมากกว่าปัจจัยเสี่ยงเพียงปัจจัยเดียว อุปสรรคดั้งเดิมในการปลูกถ่ายอวัยวะ ได้แก่ อายุที่เพิ่มขึ้น โรคอ้วน ประวัติมะเร็ง โรคร้ายแรง และโรคทางระบบร่วม แต่ปัจจัยเหล่านี้กำลังถูกท้าทายเมื่อไม่นานมานี้ อายุของผู้รับการปลูกถ่ายอวัยวะเพิ่มขึ้นอย่างต่อเนื่อง และภายในปี พ.ศ. 2564 ผู้รับ 34% ในสหรัฐอเมริกาจะมีอายุมากกว่า 65 ปี ซึ่งบ่งชี้ว่าอายุทางชีวภาพมีความสำคัญมากขึ้นกว่าอายุตามปฏิทิน ปัจจุบัน นอกเหนือจากระยะทางเดินหกนาทีแล้ว มักจะมีการประเมินภาวะเปราะบางอย่างเป็นทางการมากขึ้น โดยมุ่งเน้นไปที่การสำรองทางกายภาพและการตอบสนองต่อความเครียดที่คาดหวัง ภาวะเปราะบางสัมพันธ์กับผลลัพธ์ที่ไม่ดีหลังการปลูกถ่ายปอด และภาวะเปราะบางมักสัมพันธ์กับองค์ประกอบของร่างกาย วิธีการคำนวณภาวะอ้วนและองค์ประกอบของร่างกายยังคงพัฒนาอย่างต่อเนื่อง โดยเน้นที่ค่าดัชนีมวลกาย (BMI) น้อยลง และเน้นที่ปริมาณไขมันและมวลกล้ามเนื้อมากขึ้น เครื่องมือที่คาดว่าจะสามารถวัดภาวะกล้ามเนื้ออ่อนแรง ภาวะกล้ามเนื้อบาง และความยืดหยุ่น กำลังได้รับการพัฒนาเพื่อคาดการณ์ความสามารถในการฟื้นตัวหลังการปลูกถ่ายปอดได้ดีขึ้น การฟื้นฟูปอดก่อนการผ่าตัดสามารถปรับเปลี่ยนองค์ประกอบของร่างกายและความอ่อนแอได้ ส่งผลให้ผลลัพธ์ดีขึ้น
ในกรณีของโรควิกฤตเฉียบพลัน การประเมินระดับความอ่อนเพลียและความสามารถในการฟื้นตัวเป็นเรื่องท้าทายอย่างยิ่ง การปลูกถ่ายอวัยวะในผู้ป่วยที่ใช้เครื่องช่วยหายใจเคยพบได้น้อย แต่ปัจจุบันพบได้บ่อยขึ้น นอกจากนี้ การใช้เครื่องช่วยชีวิตนอกร่างกาย (Extracorporeal Life Support) เพื่อเป็นการรักษาระยะเปลี่ยนผ่านก่อนการปลูกถ่ายอวัยวะก็เพิ่มขึ้นในช่วงไม่กี่ปีที่ผ่านมา ความก้าวหน้าทางเทคโนโลยีและการเข้าถึงหลอดเลือดทำให้ผู้ป่วยที่มีสติสัมปชัญญะและได้รับการคัดเลือกมาอย่างดีซึ่งเข้ารับการช่วยชีวิตนอกร่างกาย สามารถเข้าร่วมกระบวนการยินยอมโดยได้รับข้อมูลอย่างครบถ้วนและการฟื้นฟูสมรรถภาพทางกาย และบรรลุผลลัพธ์หลังการปลูกถ่ายอวัยวะที่ใกล้เคียงกับผู้ป่วยที่ไม่จำเป็นต้องได้รับการช่วยชีวิตนอกร่างกายก่อนการปลูกถ่ายอวัยวะ
ก่อนหน้านี้ โรคระบบร่วม (systemic disease) ที่ถูกพิจารณาว่าเป็นข้อห้ามเด็ดขาด แต่ในปัจจุบันจำเป็นต้องประเมินผลกระทบต่อผลลัพธ์หลังการปลูกถ่ายอวัยวะโดยเฉพาะ เนื่องจากภาวะภูมิคุ้มกันบกพร่องที่เกี่ยวข้องกับการปลูกถ่ายอวัยวะเพิ่มโอกาสในการกลับเป็นซ้ำของมะเร็ง แนวทางปฏิบัติก่อนหน้านี้เกี่ยวกับโรคมะเร็งที่มีอยู่ก่อนจึงเน้นย้ำถึงข้อกำหนดที่ผู้ป่วยต้องปลอดจากมะเร็งเป็นเวลาห้าปีก่อนที่จะอยู่ในรายชื่อผู้รอการปลูกถ่ายอวัยวะ อย่างไรก็ตาม เมื่อการรักษามะเร็งมีประสิทธิภาพมากขึ้น ปัจจุบันจึงแนะนำให้ประเมินความเป็นไปได้ของการกลับเป็นซ้ำของมะเร็งตามผู้ป่วยแต่ละราย โรคภูมิต้านตนเองแบบระบบร่วม (systemic autoimmune disease) มักถูกพิจารณาว่าเป็นข้อห้าม ซึ่งเป็นมุมมองที่เป็นปัญหาเนื่องจากโรคปอดระยะลุกลามมีแนวโน้มที่จะจำกัดอายุขัยของผู้ป่วยเหล่านี้ แนวทางปฏิบัติใหม่แนะนำว่าควรประเมินและรักษาโรคที่ตรงเป้าหมายมากขึ้นก่อนการปลูกถ่ายปอด เพื่อลดอาการแสดงของโรคที่อาจส่งผลเสียต่อผลลัพธ์ เช่น ปัญหาหลอดอาหารที่เกี่ยวข้องกับโรคสเกลอโรเดอร์มา
แอนติบอดีที่ไหลเวียนต่อซับคลาส HLA เฉพาะเจาะจงอาจทำให้ผู้รับบางรายเกิดอาการแพ้อวัยวะของผู้บริจาคบางราย ส่งผลให้ระยะเวลารอคอยนานขึ้น โอกาสในการปลูกถ่ายลดลง เกิดการปฏิเสธอวัยวะเฉียบพลัน และมีความเสี่ยงต่อการเกิดภาวะ CLAD สูงขึ้น อย่างไรก็ตาม การปลูกถ่ายอวัยวะบางประเภทระหว่างแอนติบอดีของผู้รับและประเภทของผู้บริจาคให้ผลลัพธ์ที่คล้ายคลึงกันกับการรักษาด้วยการลดความไวก่อนการผ่าตัด ซึ่งรวมถึงการแลกเปลี่ยนพลาสมา อิมมูโนโกลบูลินทางหลอดเลือดดำ และการรักษาด้วยแอนติบอดีเซลล์บี
การคัดเลือกและการประยุกต์ใช้ปอดของผู้บริจาค
การบริจาคอวัยวะเป็นการกระทำที่เสียสละเพื่อผู้อื่น การได้รับความยินยอมจากผู้บริจาคและการเคารพในสิทธิของตนเองเป็นปัจจัยทางจริยธรรมที่สำคัญที่สุด ปอดของผู้บริจาคอาจได้รับความเสียหายจากการบาดเจ็บที่หน้าอก การปั๊มหัวใจ (CPR) การสำลัก การอุดตันของเส้นเลือด การบาดเจ็บหรือการติดเชื้อที่เกี่ยวข้องกับเครื่องช่วยหายใจ หรือการบาดเจ็บจากระบบประสาท ดังนั้นปอดของผู้บริจาคจำนวนมากจึงไม่เหมาะสมสำหรับการปลูกถ่าย ISHLT (สมาคมนานาชาติเพื่อการปลูกถ่ายหัวใจและปอด)
การปลูกถ่ายปอดกำหนดเกณฑ์ผู้บริจาคที่ยอมรับกันโดยทั่วไป ซึ่งแตกต่างกันไปในแต่ละศูนย์ปลูกถ่าย อันที่จริง มีผู้บริจาคเพียงไม่กี่รายที่มีคุณสมบัติตรงตามเกณฑ์ “ที่เหมาะสม” สำหรับการบริจาคปอด (รูปที่ 2) การเพิ่มการใช้ปอดของผู้บริจาคทำได้โดยการผ่อนคลายเกณฑ์ผู้บริจาค (เช่น ผู้บริจาคที่ไม่ตรงตามมาตรฐานที่เหมาะสมทั่วไป) การประเมินอย่างรอบคอบ การดูแลผู้บริจาคที่ปฏิบัติงานจริง และการประเมินในหลอดทดลอง (รูปที่ 2) ประวัติการสูบบุหรี่ของผู้บริจาคเป็นปัจจัยเสี่ยงต่อภาวะบกพร่องของการปลูกถ่ายอวัยวะขั้นต้นในผู้รับ แต่ความเสี่ยงต่อการเสียชีวิตจากการใช้อวัยวะดังกล่าวมีจำกัด และควรพิจารณาเปรียบเทียบกับผลกระทบต่อการเสียชีวิตจากการรอคอยปอดของผู้บริจาคเป็นเวลานานจากผู้ที่ไม่เคยสูบบุหรี่ การใช้ปอดจากผู้บริจาคที่มีอายุมากกว่า (อายุมากกว่า 70 ปี) ที่ได้รับการคัดเลือกอย่างเข้มงวดและไม่มีปัจจัยเสี่ยงอื่นๆ สามารถบรรลุผลสำเร็จในการรอดชีวิตและผลลัพธ์ด้านการทำงานของปอดของผู้รับได้ใกล้เคียงกับผู้บริจาคที่อายุน้อยกว่า
การดูแลอย่างเหมาะสมสำหรับผู้บริจาคอวัยวะหลายรายและการพิจารณาความเป็นไปได้ในการบริจาคปอดเป็นสิ่งสำคัญอย่างยิ่ง เพื่อให้มั่นใจว่าปอดของผู้บริจาคมีโอกาสสูงที่จะเหมาะสมสำหรับการปลูกถ่าย แม้ว่าปอดที่มีอยู่ในปัจจุบันจะมีคุณสมบัติตรงตามนิยามปอดของผู้บริจาคในอุดมคติแบบดั้งเดิมเพียงไม่กี่ปอด แต่การผ่อนคลายเกณฑ์มาตรฐานเหล่านี้อาจนำไปสู่การใช้งานอวัยวะได้อย่างมีประสิทธิภาพโดยไม่กระทบต่อผลลัพธ์ วิธีการเก็บรักษาปอดที่ได้มาตรฐานช่วยปกป้องความสมบูรณ์ของอวัยวะก่อนนำไปฝังในผู้รับ อวัยวะสามารถเคลื่อนย้ายไปยังสถานที่ปลูกถ่ายได้ภายใต้สภาวะต่างๆ เช่น การเก็บรักษาด้วยความเย็นจัด หรือการให้เลือดทางกลภายใต้ภาวะอุณหภูมิร่างกายต่ำกว่าปกติ ปอดที่ไม่ถือว่าเหมาะสมสำหรับการปลูกถ่ายทันทีอาจได้รับการประเมินเพิ่มเติมอย่างเป็นรูปธรรม และอาจได้รับการรักษาด้วยการให้เลือดทางปอดในหลอดทดลอง (in vitro lung perfusion: EVLP) หรือเก็บรักษาไว้เป็นระยะเวลานานขึ้นเพื่อเอาชนะอุปสรรคขององค์กรในการปลูกถ่าย ประเภทของการปลูกถ่ายปอด ขั้นตอน และการสนับสนุนระหว่างการผ่าตัด ล้วนขึ้นอยู่กับความต้องการของผู้ป่วย ประสบการณ์ และความต้องการของศัลยแพทย์ สำหรับผู้รับการปลูกถ่ายปอดที่มีศักยภาพซึ่งอาการแย่ลงอย่างมากในระหว่างรอการปลูกถ่าย อาจพิจารณาการช่วยชีวิตนอกร่างกายเป็นการรักษาระยะเปลี่ยนผ่านก่อนการปลูกถ่าย ภาวะแทรกซ้อนหลังการผ่าตัดในระยะแรกอาจรวมถึงภาวะเลือดออก การอุดตันของทางเดินหายใจหรือการต่อหลอดเลือด และการติดเชื้อที่บาดแผล ความเสียหายต่อเส้นประสาทเฟรนิกหรือเส้นประสาทเวกัสในทรวงอกอาจนำไปสู่ภาวะแทรกซ้อนอื่นๆ ที่ส่งผลต่อการทำงานของกะบังลมและการระบายของเสียในกระเพาะอาหารตามลำดับ ปอดของผู้บริจาคอาจมีอาการบาดเจ็บที่ปอดเฉียบพลันในระยะแรกหลังจากการฝังตัวและการกลับมาของเลือดอีกครั้ง กล่าวคือ ภาวะผิดปกติของกราฟต์ขั้นต้น การจำแนกและรักษาความรุนแรงของภาวะผิดปกติของกราฟต์ขั้นต้น ซึ่งสัมพันธ์กับความเสี่ยงสูงที่จะเสียชีวิตก่อนวัยอันควรจึงมีความสำคัญ เนื่องจากความเสียหายของปอดที่อาจเกิดขึ้นของผู้บริจาคเกิดขึ้นภายในไม่กี่ชั่วโมงหลังจากได้รับบาดเจ็บที่สมองครั้งแรก การจัดการปอดจึงควรประกอบด้วยการตั้งค่าการระบายอากาศที่เหมาะสม การขยายถุงลมปอด การส่องกล้องตรวจหลอดลม การดูดและล้างหลอดลม (เพื่อเก็บตัวอย่าง) การจัดการของเหลวของผู้ป่วย และการปรับตำแหน่งทรวงอก ABO ย่อมาจากหมู่เลือด A, B, AB และ O, CVP ย่อมาจากความดันเลือดดำส่วนกลาง, DCD ย่อมาจากผู้บริจาคปอดจากภาวะหัวใจหยุดเต้น, ECMO ย่อมาจากออกซิเจนในเยื่อหุ้มปอดนอกร่างกาย, EVLW ย่อมาจากน้ำในปอดนอกหลอดเลือด, PaO2/FiO2 ย่อมาจากอัตราส่วนของความดันออกซิเจนบางส่วนของหลอดเลือดแดงต่อความเข้มข้นของออกซิเจนที่หายใจเข้า และ PEEP ย่อมาจากความดันบวกปลายลมหายใจออก PiCCO ย่อมาจากปริมาณออกซิเจนที่หัวใจส่งออกจากรูปคลื่นดัชนีชีพจร
ในบางประเทศ การใช้ปอดผู้บริจาคที่ควบคุม (DCD) เพิ่มขึ้นเป็น 30-40% ในผู้ป่วยที่เสียชีวิตด้วยโรคหัวใจ และมีอัตราการปฏิเสธอวัยวะเฉียบพลัน CLAD และการรอดชีวิตที่ใกล้เคียงกัน โดยทั่วไป ควรหลีกเลี่ยงการปลูกถ่ายอวัยวะจากผู้บริจาคที่ติดเชื้อไวรัสติดเชื้อไปยังผู้รับที่ไม่ติดเชื้อ อย่างไรก็ตาม ในช่วงไม่กี่ปีที่ผ่านมา ยาต้านไวรัสที่ออกฤทธิ์โดยตรงกับไวรัสตับอักเสบซี (HCV) ช่วยให้สามารถปลูกถ่ายปอดผู้บริจาคที่ติดเชื้อไวรัสตับอักเสบซี (HCV) ให้กับผู้รับที่ไม่ติดเชื้อไวรัสตับอักเสบซีได้อย่างปลอดภัย ในทำนองเดียวกัน ปอดผู้บริจาคที่ติดเชื้อไวรัสเอชไอวี (HIV) สามารถปลูกถ่ายให้กับผู้รับที่ติดเชื้อไวรัสเอชไอวีได้ และปอดผู้บริจาคที่ติดเชื้อไวรัสตับอักเสบบี (HBV) สามารถปลูกถ่ายให้กับผู้รับที่ได้รับวัคซีนป้องกันไวรัสตับอักเสบบีและผู้ที่มีภูมิคุ้มกันแล้ว มีรายงานการปลูกถ่ายปอดจากผู้บริจาคที่ติดเชื้อ SARS-CoV-2 หรือเคยติดเชื้อมาก่อน เราจำเป็นต้องมีหลักฐานเพิ่มเติมเพื่อพิจารณาความปลอดภัยในการแพร่เชื้อไวรัสติดเชื้อสู่ปอดของผู้บริจาคเพื่อการปลูกถ่าย
เนื่องจากความซับซ้อนในการได้รับอวัยวะหลายชิ้น การประเมินคุณภาพของปอดผู้บริจาคจึงเป็นเรื่องท้าทาย การใช้ระบบการไหลเวียนเลือดในปอดแบบ in vitro ช่วยให้สามารถประเมินการทำงานของปอดผู้บริจาคและศักยภาพในการซ่อมแซมปอดได้อย่างละเอียดมากขึ้นก่อนนำไปใช้ (รูปที่ 2) เนื่องจากปอดผู้บริจาคมีความเสี่ยงสูงที่จะได้รับบาดเจ็บ ระบบการไหลเวียนเลือดในปอดแบบ in vitro จึงเป็นพื้นฐานสำหรับการบำบัดทางชีวภาพเฉพาะทางเพื่อซ่อมแซมปอดผู้บริจาคที่เสียหาย (รูปที่ 2) การทดลองแบบสุ่มสองชิ้นแสดงให้เห็นว่าการไหลเวียนเลือดในปอดของผู้บริจาคที่อุณหภูมิร่างกายปกติในหลอดทดลองที่ตรงตามเกณฑ์ทั่วไปมีความปลอดภัย และทีมผู้ปลูกถ่ายสามารถยืดระยะเวลาการเก็บรักษาด้วยวิธีนี้ได้ มีรายงานว่าการเก็บรักษาปอดผู้บริจาคไว้ที่อุณหภูมิต่ำกว่าปกติ (6-10°C) แทนที่จะแช่เย็นที่อุณหภูมิ 0-4°C ช่วยปรับปรุงสุขภาพของไมโทคอนเดรีย ลดความเสียหาย และปรับปรุงการทำงานของปอด สำหรับการปลูกถ่ายแบบกึ่งเลือกเฉพาะวัน มีรายงานว่าการเก็บรักษาปอดไว้ข้ามคืนนานขึ้นเพื่อให้ได้ผลลัพธ์ที่ดีหลังการปลูกถ่าย ขณะนี้กำลังมีการทดลองความปลอดภัยขนาดใหญ่ที่ไม่ด้อยกว่า โดยเปรียบเทียบการเก็บรักษาที่อุณหภูมิ 10°C กับการเก็บรักษาด้วยความเย็นมาตรฐาน (หมายเลขทะเบียน NCT05898776 ที่ ClinicalTrials.gov) ประชาชนกำลังส่งเสริมการฟื้นฟูอวัยวะอย่างทันท่วงทีมากขึ้นผ่านศูนย์ดูแลผู้บริจาคอวัยวะหลายราย และส่งเสริมการทำงานของอวัยวะผ่านศูนย์ซ่อมแซมอวัยวะ เพื่อให้สามารถใช้อวัยวะที่มีคุณภาพดีกว่าสำหรับการปลูกถ่ายอวัยวะได้ ผลกระทบของการเปลี่ยนแปลงเหล่านี้ต่อระบบนิเวศการปลูกถ่ายอวัยวะยังคงอยู่ในระหว่างการประเมิน
เพื่อรักษาอวัยวะ DCD ที่สามารถควบคุมได้ การให้เลือดที่อุณหภูมิปกติในร่างกาย ณ จุดเดิม (in situ) ผ่านการให้ออกซิเจนผ่านเยื่อหุ้มเซลล์ภายนอกร่างกาย (ECMO) สามารถนำมาใช้ประเมินการทำงานของอวัยวะในช่องท้อง และสนับสนุนการได้รับและรักษาอวัยวะทรวงอกโดยตรง รวมถึงปอด ประสบการณ์การปลูกถ่ายปอดหลังจากให้เลือดที่อุณหภูมิปกติในร่างกาย ณ จุดเดิมที่ช่องอกและช่องท้องยังมีจำกัด และผลลัพธ์ยังไม่แน่นอน มีความกังวลว่าขั้นตอนนี้อาจก่อให้เกิดอันตรายต่อผู้บริจาคที่เสียชีวิต และละเมิดหลักจริยธรรมพื้นฐานของการเก็บอวัยวะ ดังนั้น การให้เลือดที่อุณหภูมิปกติในร่างกาย ณ จุดเดิมจึงยังไม่ได้รับอนุญาตในหลายประเทศ
มะเร็ง
อัตราการเกิดมะเร็งในประชากรหลังการปลูกถ่ายปอดสูงกว่าประชากรทั่วไป และมีแนวโน้มการพยากรณ์โรคที่ไม่ดีนัก คิดเป็น 17% ของการเสียชีวิตทั้งหมด มะเร็งปอดและโรคลิมโฟโปรลิเฟอเรทีฟหลังการปลูกถ่ายปอด (PTLD) เป็นสาเหตุการเสียชีวิตจากมะเร็งที่พบบ่อยที่สุด ภาวะภูมิคุ้มกันบกพร่องระยะยาว ผลกระทบจากการสูบบุหรี่ หรือความเสี่ยงต่อการเกิดโรคปอดเรื้อรัง ล้วนนำไปสู่ความเสี่ยงในการเกิดมะเร็งปอดในปอดของผู้รับการปลูกถ่ายปอดรายเดียว แต่ในบางกรณีที่พบได้ยาก มะเร็งปอดชนิดไม่แสดงอาการที่ถ่ายทอดจากผู้บริจาคก็สามารถเกิดขึ้นได้ในปอดที่ปลูกถ่าย มะเร็งผิวหนังชนิดไม่ใช่เมลาโนมาเป็นมะเร็งที่พบบ่อยที่สุดในผู้รับการปลูกถ่าย ดังนั้นการเฝ้าระวังมะเร็งผิวหนังอย่างสม่ำเสมอจึงเป็นสิ่งจำเป็น PTLD ที่เกิดจากไวรัส Epstein-Barr เป็นสาเหตุสำคัญของโรคและการเสียชีวิต แม้ว่า PTLD จะสามารถหายได้ด้วยการกดภูมิคุ้มกันเพียงเล็กน้อย แต่มักจำเป็นต้องใช้การรักษาด้วยยา B-cell targeted therapy เช่น rituximab, เคมีบำบัดแบบระบบ หรือทั้งสองอย่าง
การอยู่รอดและผลลัพธ์ในระยะยาว
อัตราการรอดชีวิตหลังการปลูกถ่ายปอดยังคงจำกัดเมื่อเทียบกับการปลูกถ่ายอวัยวะอื่นๆ โดยมีค่ามัธยฐานอยู่ที่ 6.7 ปี และผลลัพธ์ระยะยาวของผู้ป่วยมีความก้าวหน้าเพียงเล็กน้อยตลอดระยะเวลาสามทศวรรษที่ผ่านมา อย่างไรก็ตาม ผู้ป่วยหลายรายมีคุณภาพชีวิต สภาพร่างกาย และผลลัพธ์อื่นๆ ที่ผู้ป่วยรายงานไว้ดีขึ้นอย่างมีนัยสำคัญ เพื่อให้สามารถประเมินผลการรักษาของการปลูกถ่ายปอดได้อย่างครอบคลุมมากขึ้น จำเป็นต้องให้ความสำคัญกับผลลัพธ์ที่ผู้ป่วยรายงานไว้มากขึ้น ความจำเป็นทางคลินิกที่สำคัญที่ยังไม่ได้รับการตอบสนองคือการจัดการกับการเสียชีวิตของผู้รับการปลูกถ่ายจากภาวะแทรกซ้อนร้ายแรงจากภาวะกราฟต์ล้มเหลวล่าช้าหรือภาวะภูมิคุ้มกันบกพร่องเป็นเวลานาน สำหรับผู้รับการปลูกถ่ายปอด ควรได้รับการดูแลระยะยาวอย่างจริงจัง ซึ่งต้องอาศัยความร่วมมือเป็นทีมเพื่อปกป้องสุขภาพโดยรวมของผู้รับการปลูกถ่าย โดยการติดตามและรักษาการทำงานของกราฟต์ในด้านหนึ่ง ลดผลกระทบด้านลบของภาวะภูมิคุ้มกันบกพร่อง และสนับสนุนสุขภาพกายและใจของผู้รับการปลูกถ่ายในอีกด้านหนึ่ง (รูปที่ 1)
ทิศทางในอนาคต
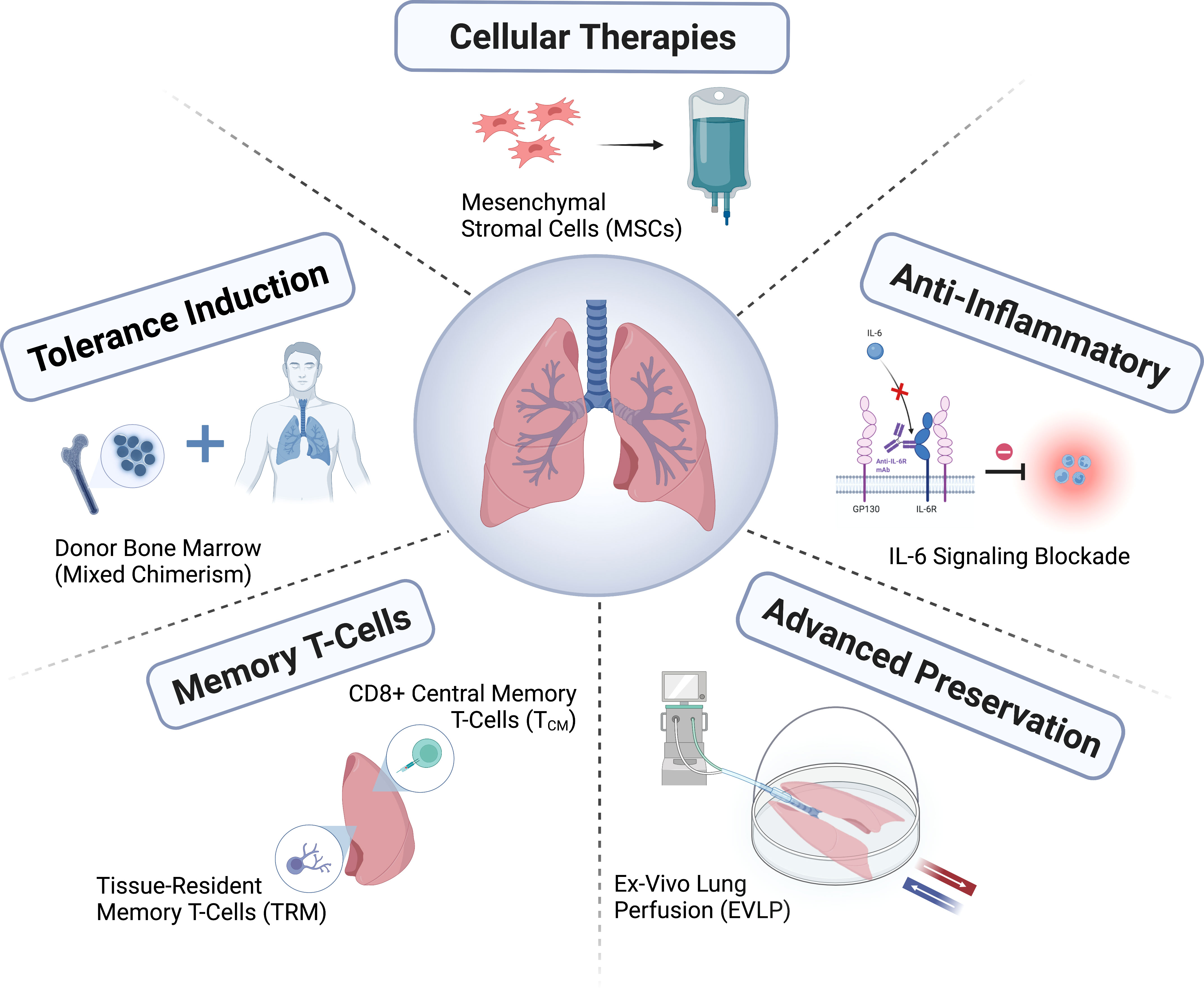
การปลูกถ่ายปอดเป็นวิธีการรักษาที่ก้าวหน้าไปมากในระยะเวลาอันสั้น แต่ยังไม่บรรลุศักยภาพสูงสุด การขาดแคลนปอดผู้บริจาคที่เหมาะสมยังคงเป็นความท้าทายสำคัญ และยังคงมีการพัฒนาวิธีการใหม่ๆ สำหรับการประเมินและดูแลผู้บริจาค การรักษาและซ่อมแซมปอดผู้บริจาค และการปรับปรุงการรักษาผู้บริจาค จำเป็นต้องปรับปรุงนโยบายการจัดสรรอวัยวะโดยการปรับปรุงการจับคู่ระหว่างผู้บริจาคและผู้รับ เพื่อเพิ่มผลประโยชน์สุทธิให้มากขึ้น ปัจจุบันมีความสนใจเพิ่มขึ้นในการวินิจฉัยภาวะปฏิเสธอวัยวะหรือการติดเชื้อผ่านการวินิจฉัยทางโมเลกุล โดยเฉพาะอย่างยิ่งกับดีเอ็นเออิสระจากผู้บริจาค หรือแนวทางการลดภาวะภูมิคุ้มกันบกพร่องให้น้อยที่สุด อย่างไรก็ตาม ประโยชน์ของการวินิจฉัยเหล่านี้ในฐานะส่วนเสริมของวิธีการติดตามการปลูกถ่ายอวัยวะทางคลินิกในปัจจุบันยังคงต้องพิจารณาต่อไป
สาขาการปลูกถ่ายปอดได้พัฒนาผ่านการจัดตั้งกลุ่มความร่วมมือ (เช่น หมายเลขทะเบียน ClinicalTrials.gov NCT04787822; https://lungtransplantconsortium.org) ซึ่งจะช่วยป้องกันและรักษาภาวะบกพร่องของกราฟต์ขั้นต้น การคาดการณ์ CLAD การวินิจฉัยและจุดภายใน (endotyping) และกลุ่มอาการที่ละเอียดขึ้น มีความก้าวหน้าอย่างรวดเร็วในการศึกษาภาวะบกพร่องของกราฟต์ขั้นต้น การปฏิเสธที่เกิดจากแอนติบอดี กลไกของ ALAD และ CLAD การลดผลข้างเคียงและลดความเสี่ยงของ ALAD และ CLAD ผ่านการรักษาด้วยภูมิคุ้มกันบำบัดเฉพาะบุคคล รวมถึงการกำหนดผลลัพธ์ที่เน้นผู้ป่วยเป็นศูนย์กลางและนำมารวมไว้ในการวัดผลลัพธ์ จะเป็นกุญแจสำคัญในการพัฒนาความสำเร็จในระยะยาวของการปลูกถ่ายปอด
เวลาโพสต์: 23 พ.ย. 2567